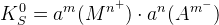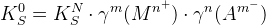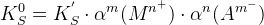Равновесие насыщенный раствор – осадок
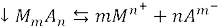
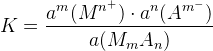
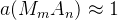 ⇒
⇒ 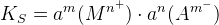
KS – произведение растворимости
Условия выпадения осадка: произведение активных концентраций больше или равно произведению растворимости:
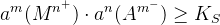
Солевые фоны увеличивают произведение растворимости.
- если осадок образован анионом сильной кислоты, то pH не влияет на произведение растворимости. Влияет реакция комплексообразования по металлу.
- если осадок образован слабой кислотой, то на произведение растворимости влияет pH (протонизация)
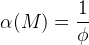
Φ – функция закомплексованности Фронеуса
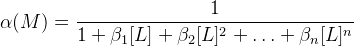
β – константа устойчивости, [L] – концентрация лиганда
Конкурирующие реакции протонизации увеличивают произведение растворимости на несколько порядков, образование комплекса – в несколько раз.
S – растворимость (моль/л, г/100г р-ля)
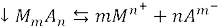
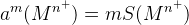
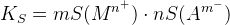
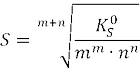 – в отсутствии солевого фона и конкурирующей реакции
– в отсутствии солевого фона и конкурирующей реакции
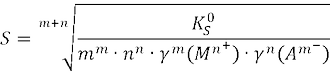
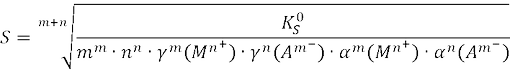
Влияние различных факторов на осаждение и растворение
Влияние избытка осадителей – избыток иона осадителей единственный фактор, уменьшающий растворимость.
Влияние гидролиза – гидролиз увеличивает растворимость
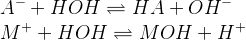
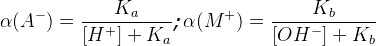
Управление процессом осаждения и растворения
Одновременное осаждение
a) для анионов сильных кислот
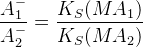 – условие одновременного выпадения осадка при отсутствии конкурирующих реакций
– условие одновременного выпадения осадка при отсутствии конкурирующих реакций
б) для анионов слабых кислот
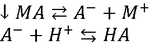
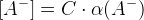 ;
; 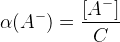 ;
; 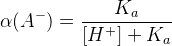
варьируя кислотность среды можно осаждать или растворять осадки
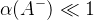
- в сильно кислых средах достигаются только низкие KS (в кислых средах осаждаются осадки с низкими KS)
- при увеличении pH α → 1,
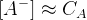 : при высоких pH достигаются высокие KS
: при высоких pH достигаются высокие KS - металл считается полностью осажденным при [M+]=10-6
формула вычисления pH осаждения: 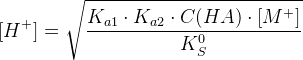
Дробное осаждение ведут при увеличении pH:
- при низких pH – малорастворимые осадки
- при высоких pH – более растворимые осадки
Условия группового осаждения – выбирают осадок с большим KS и по нему рассчитывают условия группового осаждения
Условия группового растворения – выбирают соединение с меньшим KS и рассчитывают pH
Дробное растворение – от более высокого pH к низкому
- при высоком pH растворяются осадки с высоким KS
- при низком pH растворяются осадки с низким KS
Влияние температуры – если осадок образован анионом сильной кислоты, при повышении температуры растворимость увеличивается (как правило).