Смотрите также Окислительно-восстановительное равновесие
Окислительно-восстановительные реакции (ОВР) – реакции, сопровождающиеся присоединением или отдачей электронов, или перераспределением электронной плотности на атомах (изменение степени окисления).
Стадии ОВР
Окисление – отдача электронов атомами, молекулами или ионами. В результате степень окисления повышается. Восстановители отдают электроны.
Восстановление – присоединение электронов. В результате степень окисления понижается. Окислители принимают электроны.
ОВР – сопряженный процесс: если есть восстановление, то есть и окисление.
Правила ОВР
Эквивалентный обмен электронов и атомный баланс.
Кислая среда
В кислой среде высвобождающиеся оксид-ионы связываются с протонами в молекулы воды; недостающие оксид-ионы поставляются молекулами воды, тогда из них высвобождаются протоны.
Там, где не хватает атомов кислорода, пишем столько молекул воды, сколько не хватает оксид-ионов.
Пример. Используя метод электронного баланса, составить уравнение реакции, определить окислитель и восстановитель:
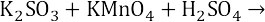
1. Определяем степень окисления: сера в сульфите калия имеет степень окисления +4, марганец в перманганате калия имеет степень окисления +7, серная кислота – среда протекания реакции.
Мараганец в высшей степени окисления – окислитель, следовательно, сульфит калия восстановитель.
Примечание: +4 – промежуточная степень окисления для серы, поэтому она может выступать как восстановителем, так и окислителем. С сильными окислителями (перманганат, дихромат) сульфит является восстановителем (окисляется до сульфата), с сильными восстановителями (галогенидами, халькогенидами) сульфит окислитель (восстанавливается до серы или сульфида).
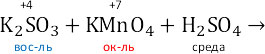
Сера из степени окисления +4 переходит в +6 – сульфит окисляется до сульфата. Марганец из степени окисления +7 переходит в +2 (кислая среда) – перманганат ион восстанавливается до Mn2+.
2. Составляем полуреакции. Уравниваем марганец: Из перманганата высвобождаются 4 оксид-иона, которые связываются ионами водорода (кислая среда) в молекулы воды. Таким образом, 4 оксид-иона связываются с 8 протонами в 4 молекулы воды.
Другими словами, в правой части уравнения не хватает 4 кислорода, поэтому пишем 4 молекулы воды, в левой части уравнения – 8 протонов.
Семь минус два – плюс пять электронов. Можно уравнивать по общему заряду: в левой части уравнения восемь протонов минус один перманганат = 7+, в правой части марганец с зарядом 2+, вода электронейтральна. Семь минус два – плюс пять электронов. Все уравнено.
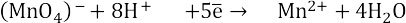
Уравниваем серу: недостающий оксид-ион в левой части уравнения поставляется молекулой воды, из которой впоследствии высвобожается два протона в правую часть.
Слева заряд 2-, справа 0 (-2+2). Минус два электрона.
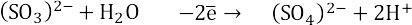
3. Суммарное уравнение электронного баланса. Умножаем верхнюю полуреакцию на 2, нижнюю на 5.
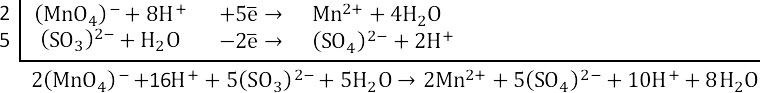
Сокращаем протоноы и воду.
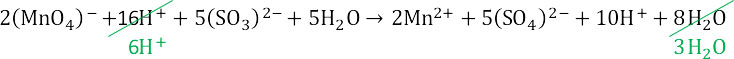
4. Итоговое уравнение реакции: Сульфат ионы связываются с ионами калия и марганца.
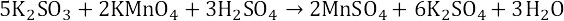
Щелочная среда
В щелочной среде высвобождающиеся оксид-ионы связываются молекулами воды, образуя гидроксид-ионы (OH– группы). Недостающие оксид-ионы поставляются гидроксо-группами, которых надо брать в два раза больше.
Там, где не хватает оксид-ионов пишем гидроксо-групп в 2 раза больше, чем не хватает, с другой стороны – воду.
Пример. Используя метод электронного баланса, составить уравнение реакции, определить окислитель и восстановитель:
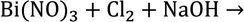
Определяем степень окисления:
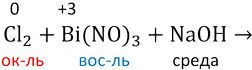
Висмут (III) с сильными окислителями (например, Cl2) в щелочной среде проявляет восстановительные свойства (окисляется до висмута V):
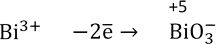
Так как в левой части уравнения не хватает 3 кислородов для баланса, то пишем 6 гидроксо-групп, а справа – 3 воды.
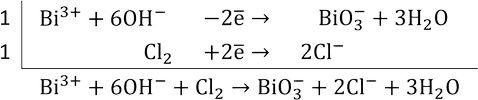
Итоговое уравнение реакции:
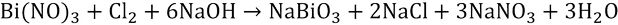
Нейтральная среда
В нейтральной среде высвобождающиеся оксид-ионы связываются молекулами воды с образованием гидроксид-ионов (OH– групп). Недостающие оксид-ионы поставляются молекулами воды. Из них высвобождаются ионы H+.
Используя метод электронного баланса, составить уравнение реакции, определить окислитель и восстановитель:
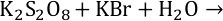
1. Определяем степень окисления: сера в персульфате калия имеет степень окисления +7 (является окислителем, т.к. высшая степень окисления), бром в бромиде калия имеет степень окисления -1 (является восстановителем, т.к. низшая степень окисления), вода – среда протекания реакции.
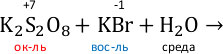
Сера из степени окисления +7 переходит в +6 – персульфат восстанавливается до сульфата. Бром из степени окисления -1 переходит в 0 – бромид ион окисляется до брома.
2. Составляем полуреакции. Уравниваем серу (коэффициент 2 перед сульфатом). Кислород уравнен.
В левой части заряд 2-, в правой части заряд 4-, присоединено 2 электрона, значит пишем +2
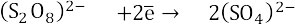
Уравниваем бром (коэффициент 2 перед бромид-ионом). В левой части заряд 2-, в правой части заряд 0, отдано 2 электрона, значит пишем –2
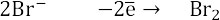
3. Суммарное уравнение электронного баланса.
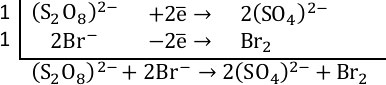
4. Итоговое уравнение реакции: Сульфат ионы связываются с ионами калия в сульфат калия, коэффициент 2 перед KBr и перед K2SO4. Вода оказалась не нужна – заключаем в квадратные скобки.
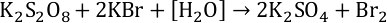
Классификация ОВР
- Окислитель и восстановитель – разные вещества
- Самоокислители, самовосстановители (диспропорционирование, дисмутация). Элемент в промежуточной степени окисления.
- Окислитель или восстановитель – среда для прохождения процесса
- Внутримолекулярное окисление-восстановление. В состав одного и того же вещества входят окислитель и восстановитель.
Твердофазные, высокотемпературные реакции.
Количесвеннная характеристика ОВР
Стандартный окислительно-восстановительный потенциал, E0 – электродный потенциал относительно стандартного водородного потенциала. Больше об окислительно-восстановительном равновесии.
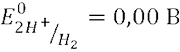
Для прохождения ОВР необходимо, чтобы разность потенциалов была больше нуля, то есть потенциал окислителя должен быть больше потенциала восстановителя:
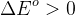 ,
, 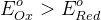
Например:

Чем ниже потенциал, тем сильнее восстановитель; чем выше потенциал, тем сильнее окислитель.
Окислительные свойства сильнее в кислой среде, восстановительные – в щелочной.
