Скачать (43 Kb)
К лекции «Химическое равновесие»
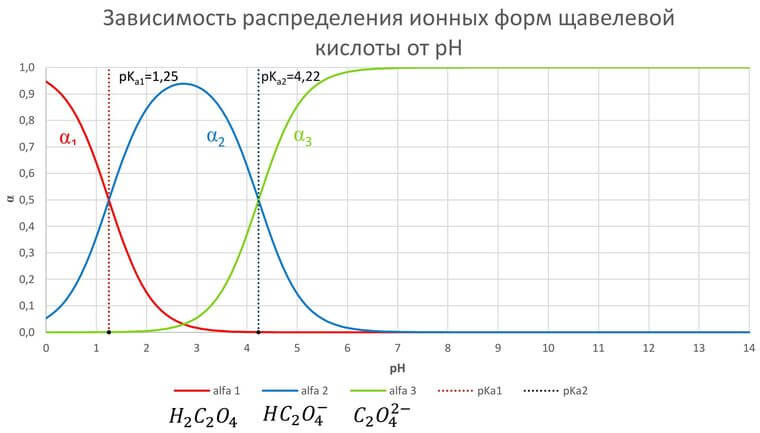
Зависимость распредления ионных форм щавелевой кислоты от pH
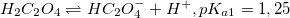
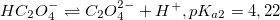
При низком pH доминирует недиссоциированная форма H2C2O4. С увеличением pH возрастает концентрация HC2O4–. Первому пересечению при pH=pKa1=1,25 соответствует равенство концентраций H2C2O4 и HC2O4–, второму (pH=pKa2=4,22) – HC2O4– и C2O42–. При pH больше 5 доминирует C2O42–.