Химические свойства моносахаридов обусловлены наличием:
- карбонильной группы (ациклическая форма моносахарида)
- полуацетального гидроксила (циклическая форма моносахарида)
- спиртовых ОН групп
Восстановление
- Продукты восстановления: многоатомные спирты –глициты
- Восстановитель: NaBH4 или каталитическое гидрирование.
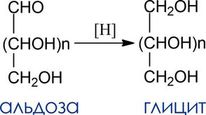
Глициты используются в качестве заменителей сахара.
При восстановлении альдоз происходит “уравнивание” функциональных групп на концах цепи. В результате из некоторых альдоз (эритрозы, рибозы, ксилозы, аллозы, галактозы) образуются оптически неактивные мезо-соединения, например. При восстановлении кетоз из карбонильной группы возникает новый хиральный центр и образуется смесь неравных количеств диастереомерных спиртов (эпимеров по С2):
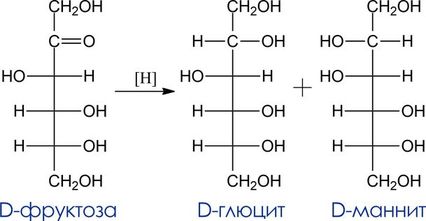
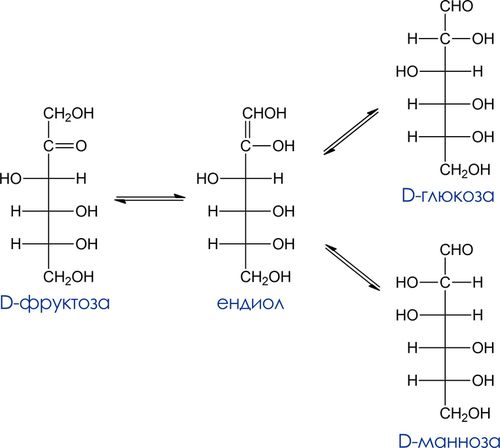
Эта реакция доказывает, что D-фруктоза, D-глюкоза и D-манноза имеют одинаковые конфигурации хиральных центров С2, С3, и С4.
Окисление
Окислению могут подвергаться:
- карбонильная группа
- оба конца углеродной цепи (карбонильная группа и гидроксогруппа у шестого атома углерода)
- гидроксогруппа у шестого атома углерода независимо от карбонильной
Вид окисления зависит от природы окислителя.
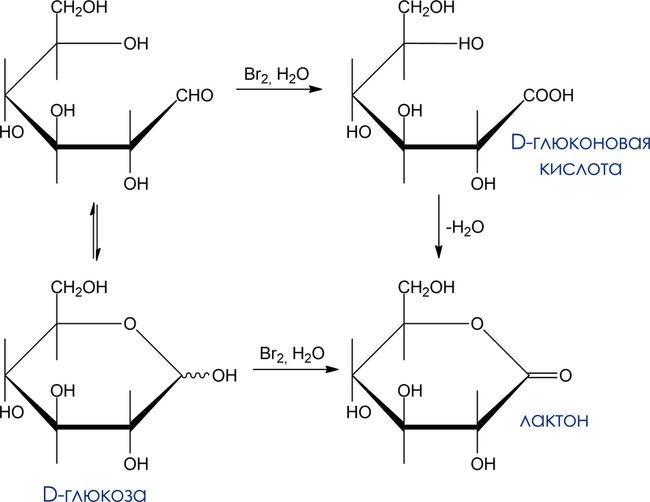
Мягкое окисление. Гликоновые кислоты
- Окислитель: бромная вода
- Что окисляется: карбонильная группа альдоз. Кетозы в этих условиях не окисляются и могут быть таким образом выделены из смесей с альдозами.
- Продукты окисления: гликоновые кислоты (из ациклических моносахаридов), пяти- и шестичленные лактоны (из циклических).
Восстанавливающие моносахариды. Качественная реакция на альдегидную группу
- Окислитель: катионы металлов Ag+ ([Ag(NH3)2]OH – реактив Толенса) и Cu2+ (комплекс Cu2+ с тартрат-ионом – реактив Фелинга) в щелочной среде
- Что окисляется: карбонильная группа альдоз и кетоз
- Продукты окисления: гликоновые кислоты и продукты деструктивного распада
Альдоза + [Ag(NH3)2]+ → гликоновая кислота + Ag + продукты деструктивного окисления
Альдоза + Cu2+ → гликоновая кислота + Cu2O + продукты деструктивного окисления
Восстанавливающие углеводы – углеводы, способные восстанавливать реактивы Толенса и Фелинга. Кетозы проявляют восстанавливающие свойства за счет изомеризации в щелочной среде в альдозы, которые и взаимодействуют далее с окислителем. Процесс превращения кетозы в альдозу происходит в результате енолизации. Образующийся из кетозы енол является общим для нее и 2-х альдоз (эпимеров по С-2). Так, в слабощелочном растворе в равновесии с D-фруктозой находятся ендиол, D-глюкоза и D-манноза.
Эпимеризация – взаимопревращения между альдозами, эпимерами по С2 в щелочном растворе.
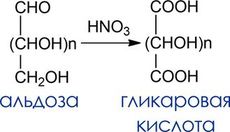
Жесткое окисление. Гликаровые кислоты
- Окислитель: разбавленная азотная кислота
- Что окисляется: оба конца углеродной цепи. Окисление кетоз азотной кислотой протекает с расщеплением С-С связей.
- Продукты окисления: гликаровые кислоты
При образовании гликаровых кислот, происходит “уравнивание” функциональных групп на концах цепи и из некоторых альдоз образуются мезо-соединения.
Ферментативное окисление в организме. Гликуроновые кислоты
- Окислитель: ферменты в организме. В лабораторных условиях для защиты карбонильной группы проводят многостадийный синтез.
- Что окисляется: гидроксогруппа у шестого атома углерода независимо от карбонильной
- Продукты окисления: гликуроновые кислоты
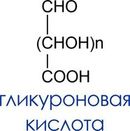
Гликуроновые кислоты входят в состав полисахаридов (пектиновые вещества, гепарин). Важная биологическая роль D-глюкуроновой кислоты состоит в том, что многие токсичные вещества выводятся из организма с мочой в виде растворимых глюкуронидов.
Реакции полуацетального гидроксила. Гликозиды
Моносахариды способны присоединять соединения различной природы с образованием гликозидов. Гликозид – молекула, в которой остаток углевода связан с другой функциональной группой посредством гликозидной связи.
В присутствии кислот моносахариды взаимодействуют с соединениями, содержащими гидроксогруппу. В результате образуются циклические ацетали – O-гликозиды.
Строение гликозидов
Молекула гликозида состоит из двух частей – углеводная компонента и агликон:
По типу связи углеводного остатка и агликона различают:
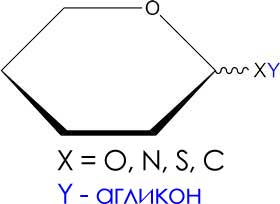
- O-гликозиды
- N-гликозиды
- C-гликозиды
- S-гликозиды
По размеру цикла гликозиды:
- пиранозиды
- фуранозиды
По природе углевода:
- глюкозиды (ацетали глюкозы)
- рибозиды (ацетали рибозы)
- фруктозиды (ацетали фруктозы)
и т. д.
По природе агликона:
- фенологликозиды
- антрахиноновые гликозиды
и т. д.
Получение гликозидов
Распространенный способ получения гликозидов – пропускание газообразного хлороводорода (катализатор) через раствор моносахарида в спирте:
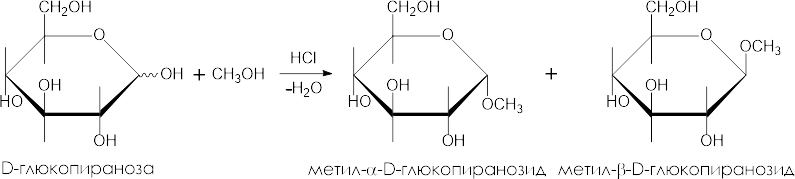
Гидролиз гликозидов
Гликозиды легко гидролизуются в кислой среде, устойчивы к гидролизу в слабощелочной среде. Фуранозиды из-за напряженности цикла гидролизуются легче пиранозидов. В результате гидролиза гликозидов образуется соответствующее гидроксосодержащее соединение (спирт, фенол и т. д.) и моносахарид.
Образование простых эфиров
При взаимодействии спиртовых гидроксогрупп с алкилгалогенидами образуются простые эфиры. Простые эфиры устойчивы к гидролизу, а гликозидная связь гидролизуется в кислой среде:
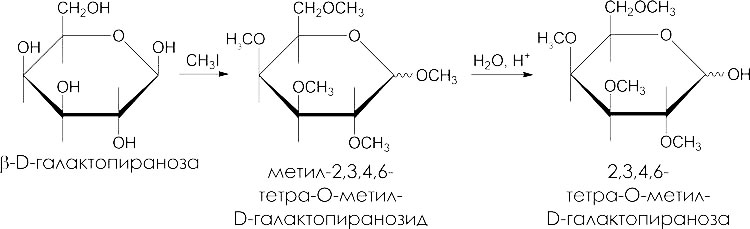
Образование сложных эфиров
Моносахариды вступают в реакцию ацилирования с ангидридами органических кислород. В результате образуются сложные эфиры. Сложные эфиры гидролизуются как в кислой, так и в щелочной средах:
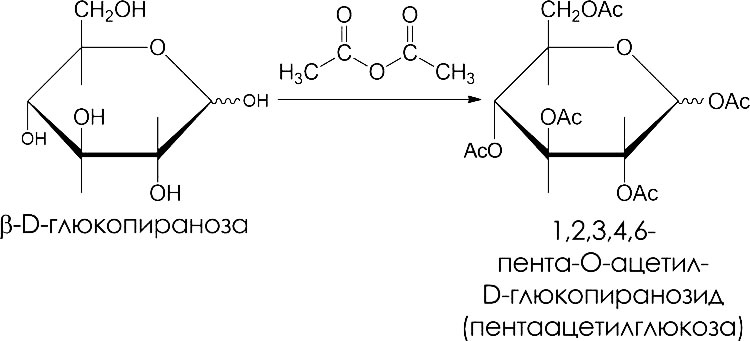
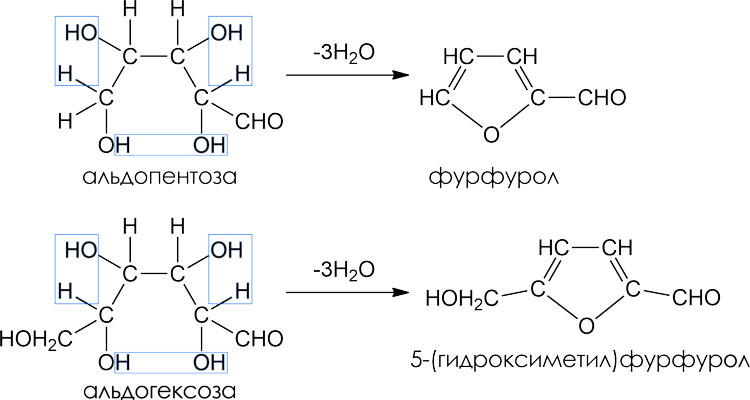
Дегидратация
Дегидратация углеводов происходит при нагревании с минеральными кислотами: